Las Partículas Subatomicas
Modelos Atómico de Bohr y Modelo Actual
Bohr unió la idea de átomo nuclear de Rutherford con las ideas de una nueva rama de la Ciencia: la Física Cuántica. Así, en 1913 formuló una hipótesis sobre la estructura atómica en la que estableció tres postulados:
¤ El electrón no puede girar en cualquier órbita, sino sólo en un cierto número de órbitas estables. En el modelo de Rutherford se aceptaba un número infinito de órbitas.
¤ Cuando el electrón gira en estas órbitas no emite energía.
¤ Cuando un átomo estable sufre una interacción, como puede ser el impacto de un electrón o el choque con otro átomo, uno de sus electrones puede pasar a otra órbita estable o ser arrancado del átomo.
¤ El electrón no puede girar en cualquier órbita, sino sólo en un cierto número de órbitas estables. En el modelo de Rutherford se aceptaba un número infinito de órbitas.
¤ Cuando el electrón gira en estas órbitas no emite energía.
¤ Cuando un átomo estable sufre una interacción, como puede ser el impacto de un electrón o el choque con otro átomo, uno de sus electrones puede pasar a otra órbita estable o ser arrancado del átomo.
El átomo de hidrógeno según el modelo atómico de Bohr
¤ El átomo de hidrógeno tiene un núcleo con un protón.
¤ El átomo de hidrógeno tiene un electrón que está girando en la primera órbita alrededor del núcleo. Esta órbita es la de menor energía.
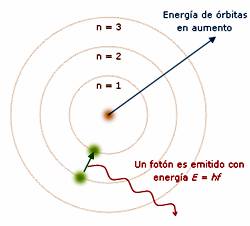
¤ Si se le comunica energía a este electrón, saltará desde la primera órbita a otra de mayor energía. cuando regrese a la primera órbita emitirá energía en forma de radiación luminosa.
¤ El átomo de hidrógeno tiene un núcleo con un protón.
¤ El átomo de hidrógeno tiene un electrón que está girando en la primera órbita alrededor del núcleo. Esta órbita es la de menor energía.
¤ Si se le comunica energía a este electrón, saltará desde la primera órbita a otra de mayor energía. cuando regrese a la primera órbita emitirá energía en forma de radiación luminosa.
En la siguiente simulación puedes elegir la órbita de giro del electrón. Observa cómo las energías de las órbitas más exteriores son mayores que las de las órbitas más interiores. "r" es el radio de la órbita.
Modelo Atómico de Dalton
El modelo atómico de Dalton, surgido en el contexto de la
química, fue el primer modelo atómico con bases científicas,
formulado en 1808 por John Dalton. El siguiente modelo fue el
modelo atómico de Thomson.
Dalton propone al átomo como una masa propia de cada elemento, combinable con otras masas propia a cada elemento, que podían ser combinados con otros, bajo las leyes de las proporciones definidas y múltiples; sin embargo su teoría no explicó la afinidad de un elemento por otro, ni la presencia de partículas subatómicas, por lo contrario siempre consideró al átomo como una masa compacta e indivisible.
De este modo establece que los elementos están formados por partículas muy pequeñas denominadas átomos y que los átomos de un mismo elemento poseen igual propiedad, tamaño y masa; no obstante según Dalton los átomos de un elemento son distintos a los de los demás elementos.

Modelo Atómico de Rutherford
El modelo atómico de Rutherford es un
modelo atómico o teoría sobre la estructura
interna del átomo propuesto por el químico
y físico británico-neozelandés Ernest
Rutherford para explicar los resultados de su
"experimento de la lámina de oro", realizado
en 1911.
El modelo de Rutherford fue el primer
modelo atómico que consideró al átomo
formado por dos partes: la "corteza",
constituida por todos sus electrones, girando
a gran velocidad alrededor de un "núcleo",
muy pequeño, que concentra toda la carga
eléctrica positiva y casi toda la masa del
átomo.

Modelo Mecánico Cuántico Actual
Es un rediseño del modelo de Bohr, ya que este solo explicaba el esprecto de emisión del hidrógeno, pero no el de otros átomos polielectronicos, ademas de que no satisfacian las direcciones privilegiadas de los enlaces químicos, como la molécula lineal del CO y la molecula angular de H2O.
Falto insertar video de Ciencias, y que creara una entrada más en la que tenia que hablar acerca de ese video
ResponderEliminar